بناء الذرة والجدول الدوري ⚛️📊
مكونات الذرة المتعادلة
لكل عنصر تركيب ذري مميز يتكون من عدد محدد من البروتونات والنيوترونات والإلكترونات. وفي الذرة المتعادلة، يكون عدد الإلكترونات مساوياً دائماً لعدد البروتونات.
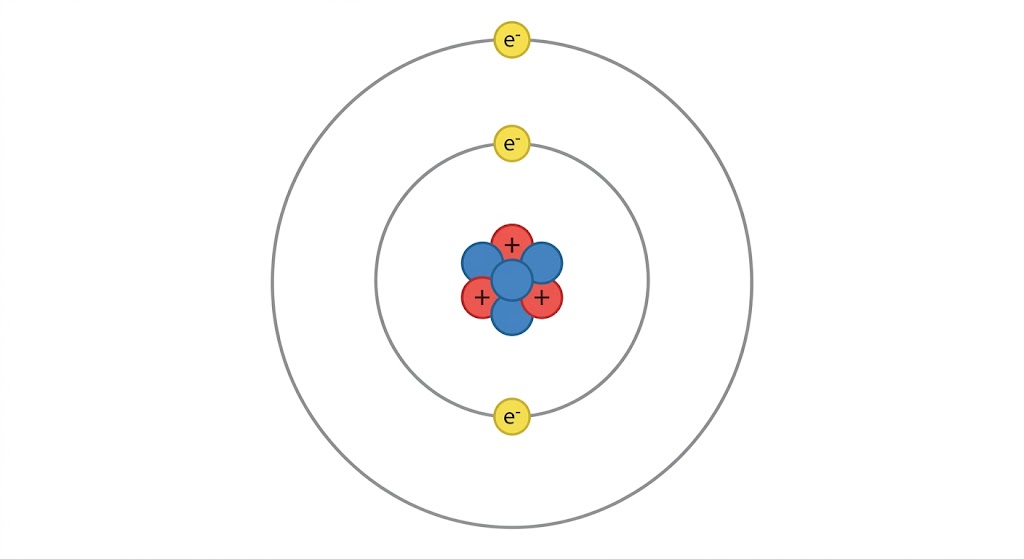
مستويات الطاقة وسعة الإلكترونات
تترتب الإلكترونات في سحابة الذرة ضمن مستويات طاقة مختلفة. تذكر هذه الحقائق الهامة حول طاقة المستوى:
- 🔹 طاقة الإلكترونات الأقرب للنواة تكون أقل ما يمكن.
- 🔹 تزداد طاقة المستوى كلما ابتعدنا عن النواة.
حسب قاعدة (2ن²)، السعة القصوى للمستويات هي:
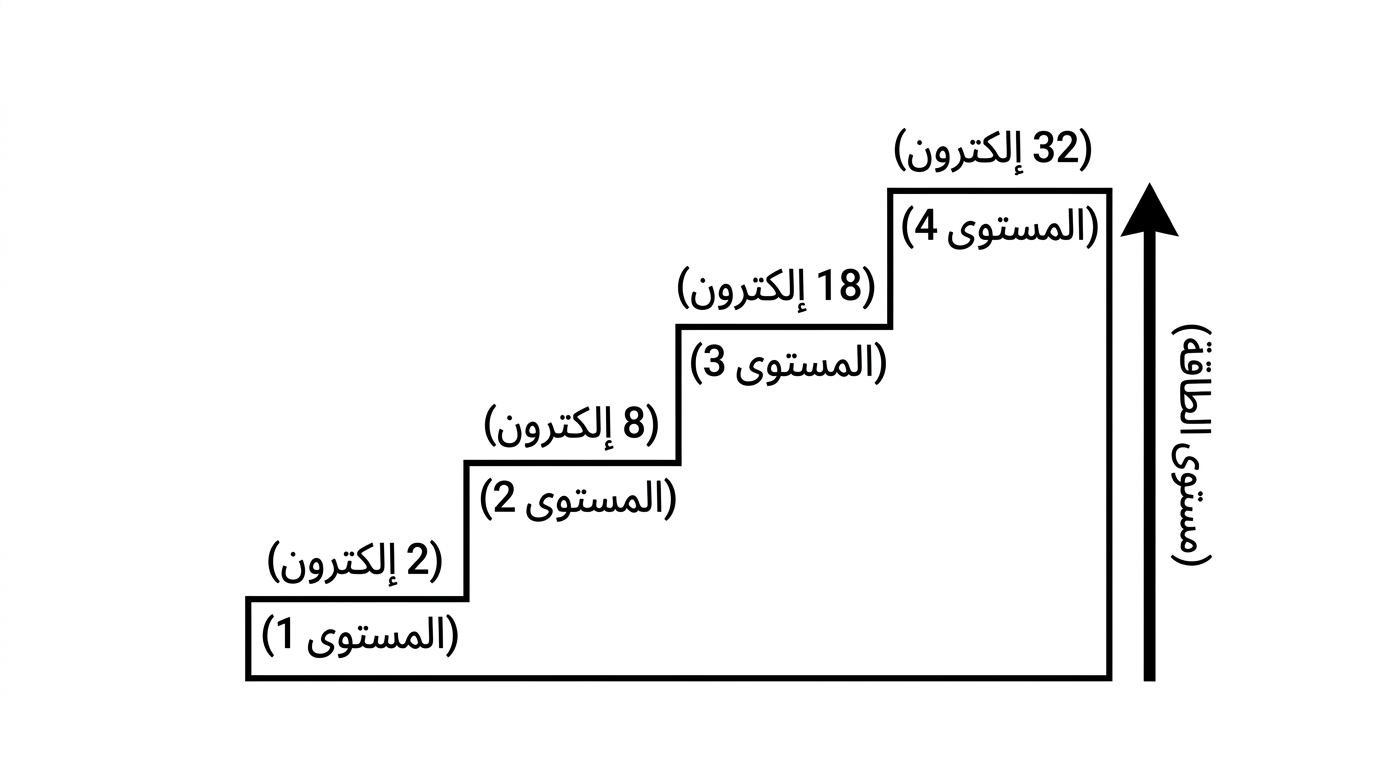
توزيع الإلكترونات في الدورات
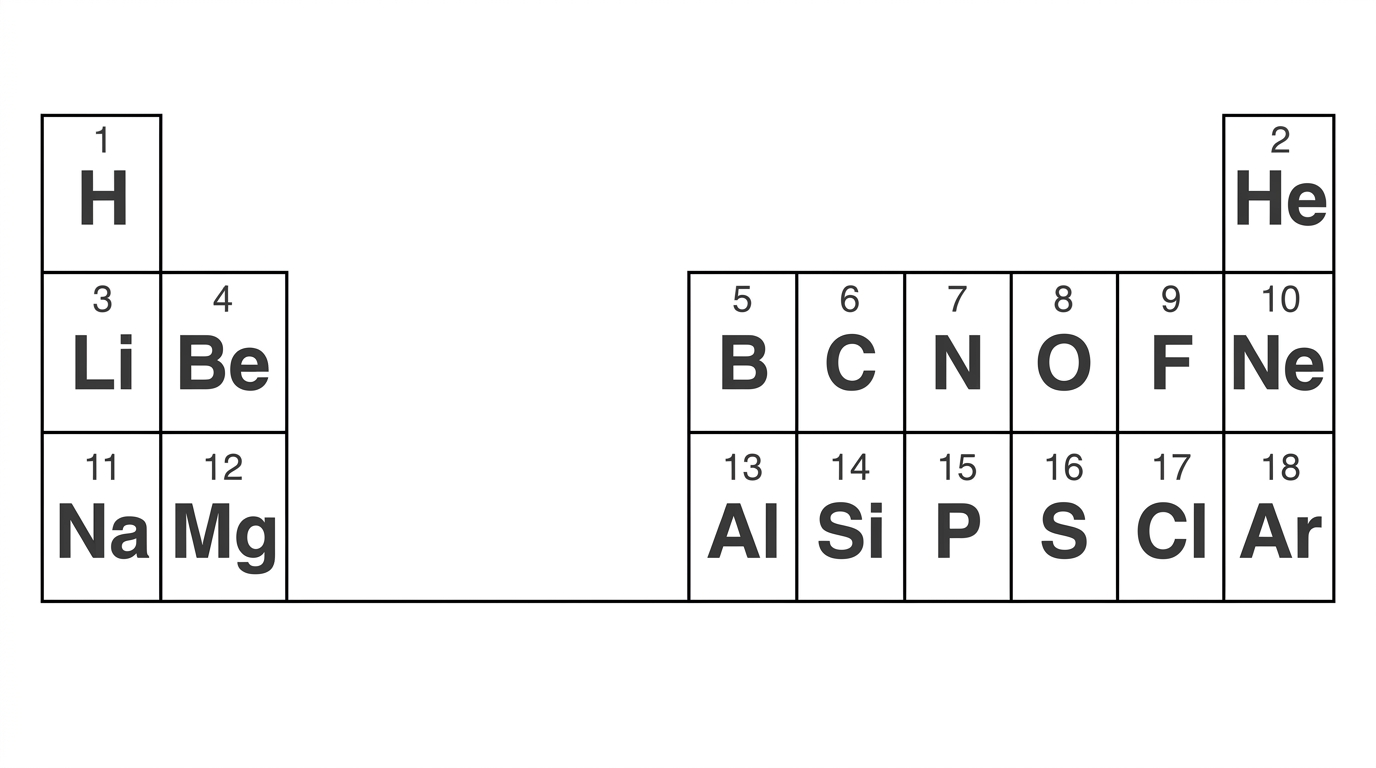
هل تعلم أن مكان العنصر في الجدول الدوري يخبرنا الكثير عن إلكتروناته؟
- رقم الدورة: يشير إلى عدد مستويات الطاقة المشغولة بالإلكترونات[cite: 247].
- التدرج: يزداد عدد الإلكترونات واحداً تلو الآخر كلما انتقلنا من اليسار إلى اليمين في الدورة[cite: 252].
- الاستقرار: تنتهي كل دورة بعنصر مستقر (مثل النيون والأرجون) لأن مستواها الخارجي مكتمل بـ 8 إلكترونات.
ملاحظة هامة حول الاستقرار:
يصل العنصر لحالة الاستقرار عندما يكتمل مستواه الخارجي، حيث يستقر مستوى الطاقة الأول بإلكترونين، بينما يستقر المستوى الثاني بـ 8 إلكترونات، و المستوى الثالث بـ 8 إلكترونات.
ملخص الدرس
- ⚛️ الذرة المتعادلة: بروتونات (+) = إلكترونات (-).
- 🔋 الطاقة تزداد كلما ابتعد مستوى الطاقة عن النواة.
- 🪜 قاعدة (2ن²) تحدد سعة المستويات (2، 8، 18، 32).
- 🏁 كل دورة في الجدول الدوري تنتهي بعنصر مستقر ذو مستوى خارجي مكتمل.
أحسنت يا عالم المستقبل!
لقد أتقنت أساسيات بناء المادة وتوزيع إلكتروناتها وطاقتها.

