التفاعلات والمعادلات الكيميائية 🧪💥
كيف نميز التفاعل؟
تتعرض المادة لنوعين من التغيرات:
🧊 تغير فيزيائي
يؤثر في الخصائص الفيزيائية فقط (الحجم، الشكل، الحالة) دون تغيير هوية المادة. مثل تجمد الماء.
🔥 تغير كيميائي
ينتج مادة جديدة بخصائص مختلفة تماماً عن الأصلية. وتسمى هذه العملية التفاعل الكيميائي.
من دلالات التفاعل الكيميائي: تصاعد الفقاقيع، الرائحة، تغير اللون، أو إنتاج طاقة ضوئية كما في الحشرات المضيئة.

مكونات المعادلة الكيميائية
1. معادلة لفظية:
2. معادلة بالصيغ الكيميائية:
الأرقام السفلية: تعبر عن عدد ذرات كل عنصر في المركب. فمثلاً في CO₂ الرقم (2) يعني وجود ذرتين من الأكسجين.
دلالات الرموز
| الرمز | الدلالة |
|---|---|
| ➡️ | اتجاه سير التفاعل |
| ↔️ | تفاعل عكسي |
| ⬇️ | مادة مترسبة |
| ⬆️ | تصاعد غاز |
| 🔼 | حرارة (تسخين) |
| (s) | صلب |
| (l) | سائل |
| (g) | غاز |
| (aq) | محلول مائي |
النشاط الكيميائي للعناصر
تختلف العناصر في قدرتها على التفاعل. يحل العنصر الأكثر نشاطاً محل العنصر الأقل نشاطاً في محاليله.
الكتلة لا تفنى ولا تستحدث
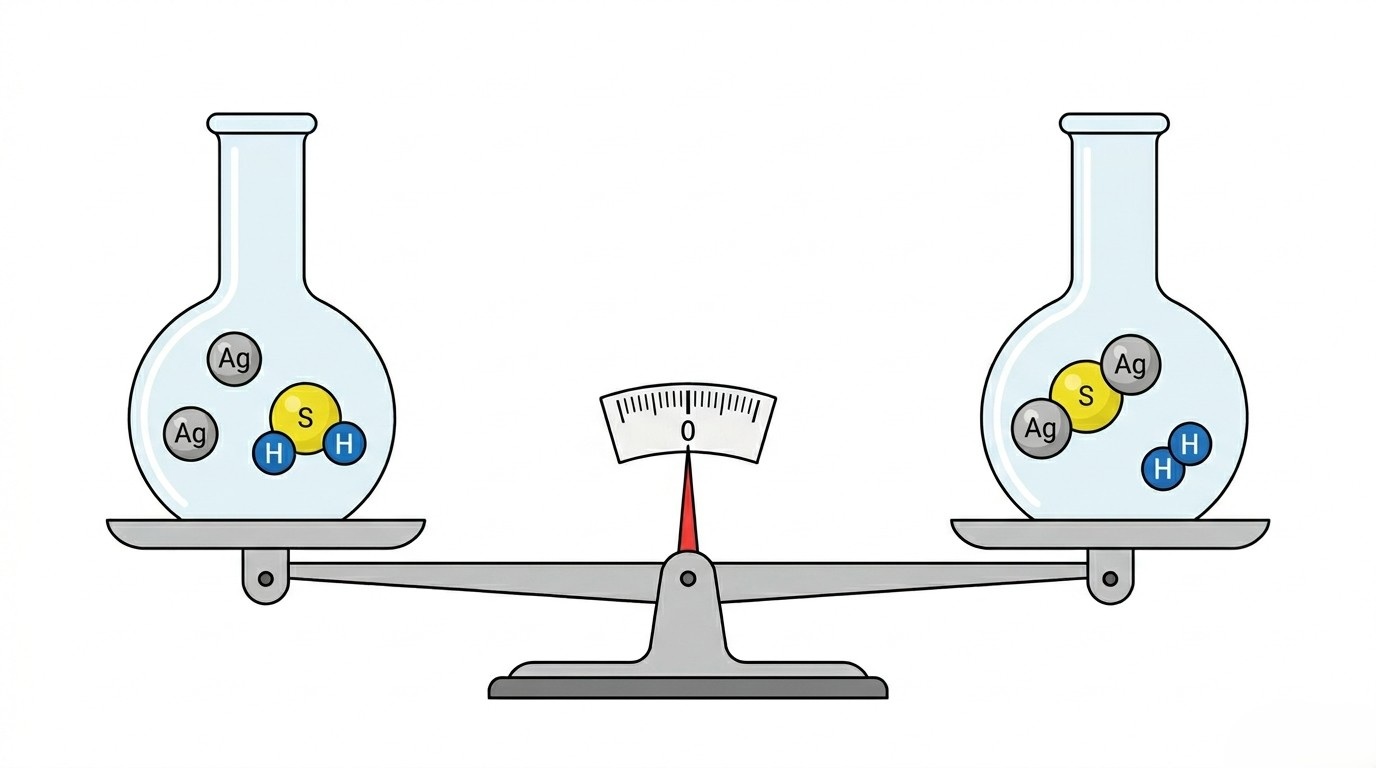
بموجب قانون حفظ الكتلة، يجب أن يتساوى عدد الذرات في طرفي المعادلة:
Ag + H₂S ➡️ Ag₂S + H₂
2Ag + H₂S ➡️ Ag₂S + H₂
⚠️ تحذير: لا تغير الأرقام السفلية أبداً، لأن ذلك يغير نوع المركب!
Mg + 2HCl ➡️ MgCl₂ + H₂
ملخص رحلتنا اليوم
- التفاعل الكيميائي: عملية كسر روابط وتكوين روابط جديدة لإنتاج مواد مختلفة.
- المتفاعلات والنواتج: أركان المعادلة الأساسية التي تفصل بينها لغة الرموز.
- النشاط الكيميائي: سلسلة تحدد قدرة العناصر على الإحلال والتفاعل.
- قانون حفظ الكتلة: القاعدة الذهبية التي تفرض موازنة المعادلة ليتساوى الطرفان.
مبدع يا بطل الكيمياء!
لقد أتممت الدرس الأول من الفصل التاسع بنجاح. أنت الآن تتقن لغة الكيمياء وقوانينها!

